近期,本学院王丽副教授课题组报道了两种超灵敏检测miRNA的电化学发光传感器,相关成果以“A tandem DNA nanomachines-supported electrochemiluminescence assay for attomolar detection of miRNA at ambient-temperature”和“Poly(3,4-ethylenedioxythiophene):poly(styrene sulfonate) modified metal-organic frameworks boosting carbon dots electrochemiluminescence emission for sensitive miRNA detection”为题分别发表在化学工程杂志(Chemical Engineering Journal,工程技术与化学化工领域顶级期刊)和生物传感器和生物电子学(Biosensors and Bioelectronics,一区TOP期刊,工程技术-电化学综合研究国际期刊)上(https://doi.org/10.1016/j.cej.2023.148161;https://doi.org/10.1016/j.bios.2024.116015)。21级硕士生彭嘉欣和王红红分别为文章的第一作者。
基于级联DNA nanomachine的方法设计:
将串联的DNA nanomachine(DNA Walker、DNA rolling machine)与电化学发光(Electrochemiluminescence, ECL)技术相结合,开发了一种超灵敏、快速、简便地检测miRNA-155方法。该策略包括在DNA轨道功能化电极上设计DNAzyme驱动的DNA Walker和催化发夹组装(catalytic hairpin assembly,CHA)驱动的DNA rolling machine。检测从DNA Walker放大开始,靶标链置换激活的DNAzyme不断切割AuNPs上底物链的腺苷酸下游(3’方向)的磷酸二酯键,使DNA Walker形成球形核酸(spherical nucleic acids,SNA)。之后,生成的SNA在电极上沿着发夹DNA轨道不断滚动并触发CHA反应,实现了信号二次放大和ECL信号读出。通过测量ECL强度对靶标miRNA-155进行定量。值得注意的是,由于DNA Walker和DNA rolling machine的原理分别基于DNAzyme的裂解和CHA,串联DNA nanomachine的信号放大过程无酶参与,整个过程可在室温下操作。与现有的DNA nanomachine检测方法相比,该检测方法取得了两个关键性的进步:(a)操作简单,反应迅速,整个检测过程只需孵育和离心步骤,在室温下约70分钟即可完成。(b)灵敏度高,对miRNA-155的检测限低至0.33aM。
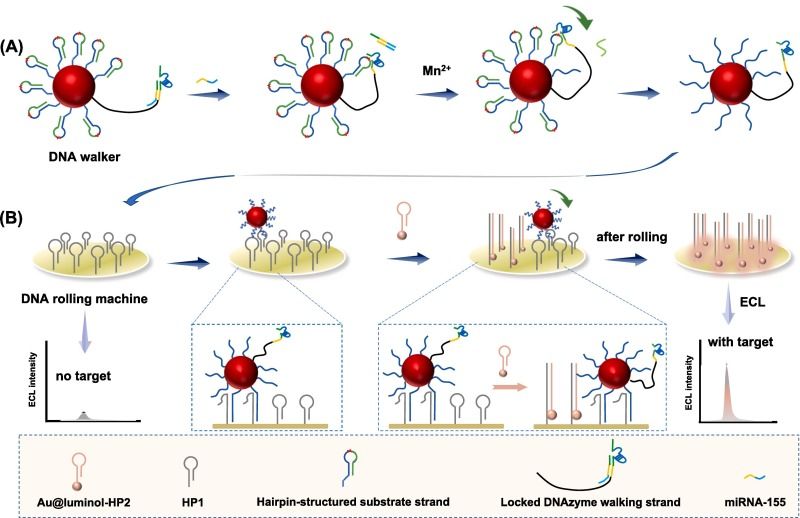
串联DNA nanomachine支持的ECL检测miRNA-155的原理
CDs/PEDOT:PSS/ZIF-8/AuNPs纳米材料作为ECL发射体的检测方法设计:
本研究合成了PEDOT:PSS修饰的CDs/ZIF-8作为高效ECL发射器,该新型发射体具有如下特性:(a)ZIF-8的拓扑秩序和多孔结构使CDs在框架内定位和均匀分布;(b)高导电性PEDOT:PSS和AuNPs促进了纳米材料和电极之间的电子转移,促进了吸附在ZIF-8框架中的CDs的电化学活化。因此,所制备的CDs/PEDOT:PSS/ZIF-8/AuNPs显示出比单个CDs高10倍的ECL发射。基于CDs/PEDOT:PSS/ZIF-8/AuNPs优异的ECL性能和易于标记的特性,将新型复合材料与基于DNAzyme的双循环靶扩增相结合,成功构建了一种新型ECL生物传感器,实现了对miRNA-21的超灵敏、高选择性测定,LOD低至50 aM。
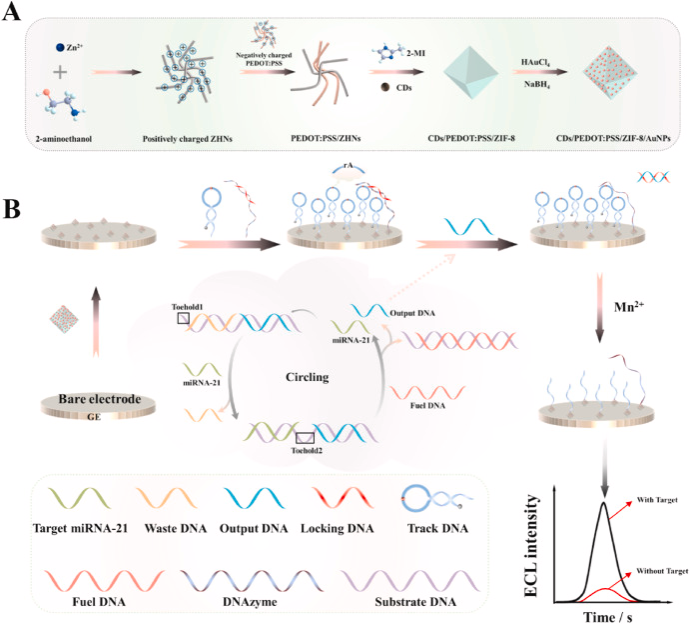
(A)CDs/PEDOT:PSS/ZIF-8/AuNPs的制备工艺。(B)用于miRNA-21检测的ECL生物传感器示意图。
总的来说,构建了两种超灵敏的电化学发光生物传感器,用于无扩增miRNA检测。检测miRNA-155和miRNA-21的LOD分别为0.33 aM和50 aM。